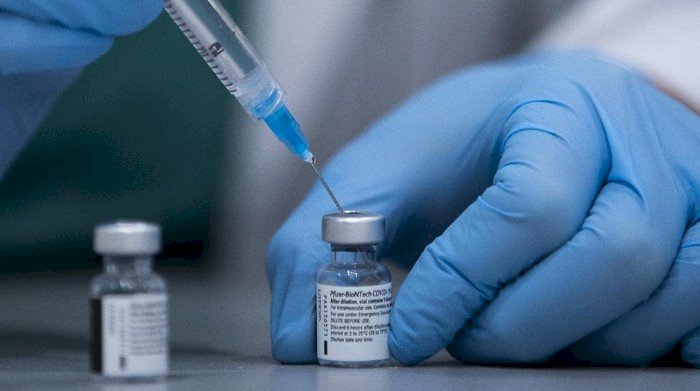
Menambah dari jenis vaksin COVID-19 yang ada saat ini, Badan Pengawas Obat dan Makanan (BPOM) kembali menerbitkan Emergency Use Authorization (EUA) untuk salah satu jenis vaksin dari platform mRNA, Rabu (14/7).
Menambah dari jenis vaksin COVID-19 yang ada saat ini, Badan Pengawas Obat dan Makanan (BPOM) kembali menerbitkan Emergency Use Authorization (EUA) untuk salah satu jenis vaksin dari platform mRNA, Rabu (14/7).
- Sumsel Dapat Alokasi Vaksin Booster Kedua, Ini Jumlahnya
- OKU Minta Tambahan 3.000 Dosis Vaksin Jenis Pfizer dan Moderna
- Vaksin Covid-19 Pfizer Ampuh 73,2 Persen Efektif untuk Anak Usia di Bawah 5 tahun
Baca Juga
“Badan POM telah menerbitkan EUA untuk satu jenis vaksin COVID-19 yang dikembangkan dengan platform mRNA, yaitu Vaksin Comirnaty yang diproduksi Pfizer and BioNTech,” kata Kepala Badan POM Penny K. Lukito saat konferensi pers virtual Kamis (15/7/2021).
Lanjutnya, vaksin ini digunakan dengan indikasi pencegahan COVID-19 yang disebabkan oleh SARS-CoV-2 untuk orang berusia 12 tahun ke atas. Diberikan secara injeksi intramuscular, dosis 0,3 mL dengan dua kali penyuntikan dalam rentang waktu tiga minggu.
Berdasarkan data uji klinik fase tiga, efikasi vaksin Pfizer pada usia 16 tahun ke atas menunjukan keberhasilan sebanyak 95,5 persen dan pada remaja usia 12-15 tahun sebesar 100 persen.
Data imunogenisitas menunjukkan pemberian dua dosis vaksin Comirnaty dalam selang tiga minggu menghasilkan respons imun yang baik. Selain itu, hasil pengkajian menunjukan bahwa secara umum keamanan vaksin dapat ditoleransi pada semua kelompok usia.
Kejadian reaksi yang paling sering timbul dari penggunaan vaksin ini, antara lain nyeri pada tempat suntikan, kelelahan, sakit kepala, nyeri otot, menggigil, nyeri sendi, dan demam.
Penny mengatakan sebagaimana vaksin dengan platform mRNA yang memiliki spesifikasi penyimpanan khusus dengan menggunakan ultra low temperature (suhu -90° sampai -60° C) vaksin ini tentu perlu dikawal dalam proses pendistribusiannya.
“PT. Pfizer sebagai produsen telah menyiapkan sarana dan prasarana yang dibutuhkan sampai ke titik penyuntikan (tempat pelaksanaan vaksinasi) di Indonesia,” kata Penny. 
- Kasus Korupsi Pengadaan APD Covid-19, Dirut PT EKI Diperiksa KPK
- Tersangka Kasus Korupsi APD Covid-19 Diperiksa KPK
- KPK Kembali Periksa Tiga Saksi Terkait Korupsi APD Covid-19